Bộ Y tế phê duyệt có điều kiện vắc xin Covid-19 Moderna
(THPL) - Bộ Y tế có quyết định phê duyệt vắc-xin Covid-19 Spikevax (vắc-xin Moderna) do nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 tại Việt Nam.
Bộ Y tế vừa có quyết định phê duyệt có điều kiện vắc xin cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 theo quy định tại Điều 67 Nghị định số 54/2017/NĐ-CP ngày 8/5/2017 của Chính phủ quy định chi tiết một số điều và biện pháp thi hành Luật dược (Nghị định 54/2017/NĐ-CP), cụ thể:
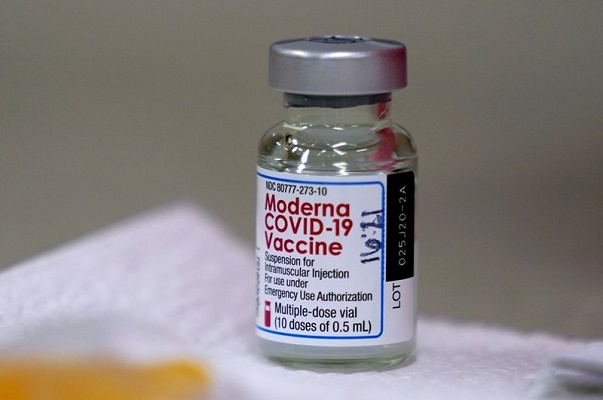
Tên vắc xin: Spikevax (Tên khác là: Covid-19 Vaccine Moderna).
Thành phần hoạt chất, nồng độ/hàm lượng: Mỗi liều 0,5ml chứa 100mcg mRNA (được nhúng trong các lipid nanoparticle SM-102).
Dạng bào chế: Hỗn dịch tiêm bắp.
Quy cách đóng gói: Hộp chứa 10 lọ đa liều; mỗi lọ đa liều chứa 10 liều 0,5ml.
Tên cơ sở sản xuất - Nước sản xuất: Rovi Pharma Industrial Services, S.A - Tây Ban Nha; Recipharm Monts - Pháp.
Cơ sở sản xuất vắc xin Spikevax khác có thể được thay đổi căn cứ vào khả năng cung cấp vắc xin tại thời điểm cơ sở nhập khẩu nộp Hồ sơ đề nghị cấp phép nhập khẩu vắc xin theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP.
Tên cơ sở đề nghị phê duyệt vắc xin: Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam.
Bộ Y tế yêu cầu Cục Quản lý Dược có trách nhiệm: Cấp phép nhập khẩu vắc xin Spikevax theo quy định tại Điều 67 Nghị định 54/2017/NĐ-CP khi nhận được hồ sơ của cơ sở nhập khẩu; Thực hiện đúng quy định của pháp luật về quản lý nhập khẩu, quản lý chất lượng vắc xin nhập khẩu.
Cục Khoa học công nghệ và Đào tạo có trách nhiệm: Lựa chọn đơn vị có đủ điều kiện đánh giá tính an toàn, hiệu quả của vắc xin trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vắc xin, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng; Hướng dẫn, chỉ đạo đơn vị có đủ điều kiện quy định tại Điểm a Khoản này tổ chức thực hiện việc đánh giá tính an toàn, hiệu quả của vắc xin Spikevax trên cơ sở ý kiến tư vấn của Hội đồng tư vấn sử dụng vắc xin, sinh phẩm y tế của Bộ Y tế trong quá trình sử dụng.
Cục Y tế Dự phòng thực hiện các trách nhiệm liên quan đến tiêm chủng vắc xin Spikevax được quy định tại Quyết định số 1464/QĐ-BYT ngày 05/03/2021 của Bộ trưởng Bộ Y tế về việc ban hành hướng dẫn tiếp nhận, bảo quản, phân phối và sử dụng vắc xin phòng Covid-19 và Quyết định số 1467/QĐ-BYT ngày 05/03/2021 của Bộ trưởng Bộ Y tế về việc phê duyệt kế hoạch tiêm vắc xin phòng Covid-19 giai đoạn 2021 - 2022.
Bộ Y tế cũng yêu cầu Chi nhánh Công ty TNHH Zuellig Pharma Việt Nam phải phối hợp với Bộ Y tế Việt Nam để triển khai quản trị rủi ro đối với vắc-xin Spikevax trong suốt quá trình lưu hành tại Việt Nam. Đồng thời, việc sử dụng vắc-xin Spikevax phải theo hướng dẫn của Bộ Y tế Việt Nam.
Như vậy, đến nay đã có 5 loại vắc-xin Covid-19 được Bộ Y tế phê duyệt có điều kiện vắc-xin cho nhu cầu cấp bách trong phòng, chống dịch bệnh Covid-19 gồm: Vắc-xin Astra Zeneca; vắc-xin Sputnick; vắc-xin Pfirez; vắc-xin Vero Cell và vắc-xin Spikevax (vắc-xin Moderna).
Tuấn Minh (tổng hợp)
Tin khác

Giá trên 540 triệu đồng, Honda Africa Twin 2026 có mặt tại Việt Nam

Mở rộng quan hệ hợp tác với Stellantis, Thaco Auto chính thức phân phối thêm 2 thương hiệu JEEP & RAM

Xăng sinh học E10: Lợi ích kép cho kinh tế và môi trường

Dự báo thời tiết ngày 2/6: Cả nước nắng nóng, nhiều nơi trên 37 độ C

Thương hiệu sữa Bellamy’s Organic trở thành Nhà tài trợ chính thức của FIFA World Cup 2026™

Quảng Ninh công bố Quyết định đặc xá năm 2026
Quảng Ninh thông qua 7 Nghị quyết quan trọng, tạo động lực phát triển bền vững
(THPL) - Với sự thống nhất tuyệt đối, Kỳ họp thứ 3 HĐND tỉnh Quảng Ninh khóa XV đã quyết nghị thông qua 7 Nghị quyết quan trọng mang tính...02/06/2026 07:05:15Quảng Ninh: Lan tỏa yêu thương, chăm lo cho trẻ em nhân Ngày Quốc tế Thiếu nhi 1/6
(THPL) – Nhân dịp Ngày Quốc tế Thiếu nhi 1/6 và hưởng ứng Tháng hành động vì trẻ em năm 2026, tỉnh Quảng Ninh đã tổ chức nhiều hoạt...01/06/2026 21:21:11Bầu Thụy ra mắt SCEX – Công ty Tài sản Mã hóa SACOM chính thức bước vào thị trường tài sản số
(THPL) - Công ty Cổ phần Sàn Giao dịch Tài sản Mã hóa Sacom (SCEX) vừa công bố lễ ra mắt các thành viên HĐQT với sự tham gia của nhiều lãnh đạo...01/06/2026 18:03:0025 triệu thuê bao di động có nguy cơ bị khóa sau ngày 15/6
(THPL) - Hiện vẫn còn khoảng 25 triệu thuê bao di động chưa thực hiện xác nhận trạng thái sở hữu chính chủ trên ứng dụng VNeID. Theo quy...01/06/2026 18:31:03
ĐỌC NHIỀU NHẤT
Quảng bá thương hiệu Việt
-

Tăng cường quảng bá sản phẩm, thương hiệu địa phương tại Hội chợ Mùa Xuân lần thứ nhất năm 2026
- Triển lãm “Đạo học ngàn năm” tôn vinh truyền thống hiếu học của dân...
- Tháo gỡ “điểm nghẽn” để ngành kim hoàn - đá quý Việt Nam cất cánh
- Vinh danh Nghệ nhân “Bàn tay vàng” và phong tặng Nghệ nhân Quốc gia






